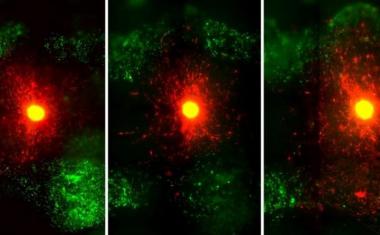
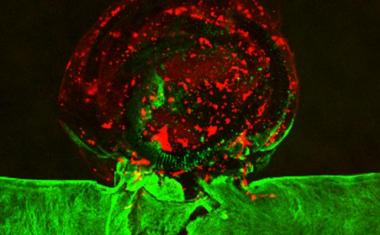
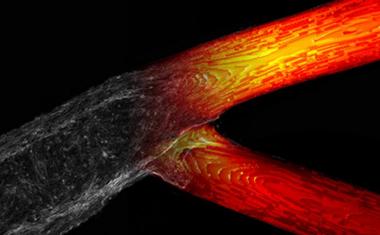
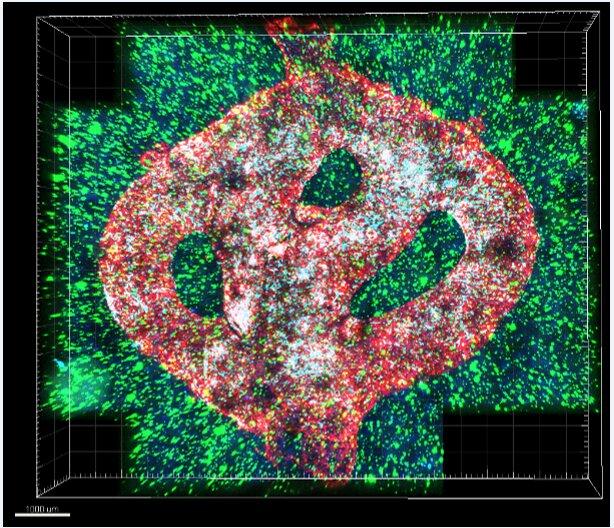
 3d生物打印胶质母细胞瘤模型显微镜图像。生物打印的血管被内皮细胞(红色)和周细胞(青色)覆盖。血管周围环绕着一个模拟大脑的组织,该组织由胶质母细胞瘤细胞(蓝色)和大脑微环境细胞(绿色)组成。不同的药物或细胞可以通过3d生物打印血管灌注,以测试它们对肿瘤组织的影响。
3d生物打印胶质母细胞瘤模型显微镜图像。生物打印的血管被内皮细胞(红色)和周细胞(青色)覆盖。血管周围环绕着一个模拟大脑的组织,该组织由胶质母细胞瘤细胞(蓝色)和大脑微环境细胞(绿色)组成。不同的药物或细胞可以通过3d生物打印血管灌注,以测试它们对肿瘤组织的影响。活性胶质母细胞瘤肿瘤首次3d生物打印
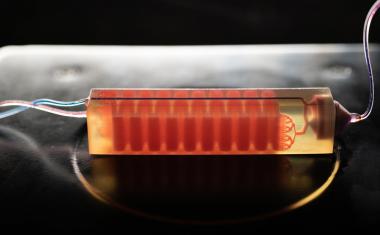
特拉维夫大学的研究人员使用3D打印机打印出了一个完整的活跃的、可存活的胶质母细胞瘤。这种3d生物打印肿瘤包括一个复杂的血管状管道系统,血细胞和药物可以通过管道流动,模拟真实的肿瘤。
这项研究由罗妮特·萨奇-法纳罗教授领导。这项新技术是由博士生莉娜·纽菲尔德(Lena Neufeld)和萨奇-法纳罗教授实验室的其他研究人员共同开发的。的3 d-bioprinted这些模型是基于直接从特拉维夫索拉斯基医疗中心的手术室采集的病人样本。
为了解决这个问题,该研究小组由Satchi-Fainaro教授和博士生莉娜Neufeld医生接受著名的丹•大卫奖学金创造了第一个3 d-bioprinted模型胶质母细胞瘤的肿瘤,包括3 d癌组织周围的细胞外基质,通过功能与它的微环境血管.
“不仅仅是癌细胞,”萨奇-法纳罗教授解释说。“这也是大脑微环境中的细胞;星形胶质细胞,小胶质细胞和血管连接到一个微流控系统也就是说,这个系统可以让我们向肿瘤复制体输送血细胞和药物等物质。每个模型都是在我们在实验室设计的生物反应器中打印出来的,使用从患者身上提取的细胞外基质中取样和复制的水凝胶,从而模拟组织本身。大脑的物理和机械特性不同于其他器官,如皮肤、乳房或骨骼。乳房组织主要由脂肪组成,骨组织主要由钙组成;每个组织都有自己的特性,这些特性会影响癌细胞的行为以及它们对药物的反应。在相同的塑料表面种植所有类型的癌症并不是临床环境的最佳模拟。”

在成功打印出3D肿瘤后,Satchi-Fainaro教授和她的同事证明,与在培养皿上生长的癌细胞不同,3D生物打印模型有潜力对特定患者快速、稳健和可重复性的最适合治疗进行有效预测。
“我们证明,我们的3D模型以三种不同的方式更适合预测治疗效果、靶点发现和药物开发。首先,我们在2D培养皿中测试了一种抑制我们最近发现的蛋白质p -选择素的物质,并发现处理过的胶质母细胞瘤细胞与未处理过的对照组细胞在细胞分裂和迁移方面没有差异。相比之下,在动物模型和3d生物打印模型中,我们能够通过阻断p -选择素蛋白来延缓胶质母细胞瘤的生长和侵袭。这个实验告诉我们为什么潜在有效的药物很少进入临床,仅仅因为它们在2D模型中测试失败,反之亦然:为什么药物在实验室中被认为是显著的成功,但最终在临床试验中失败。此外,我们与TAU医学院病理系Asaf Madi博士的实验室合作,进行了基因测序将3d生物打印模型中生长的癌细胞与2D塑料模型中生长的癌细胞和从患者身上提取的癌细胞进行比较。因此,我们证明了3d生物打印肿瘤与患者来源的胶质母细胞瘤细胞在其自然环境中与脑基质细胞一起生长有更大的相似性。随着时间的推移,生长在塑料上的癌细胞发生了很大的变化,最终失去了与病人脑瘤样本中的癌细胞的任何相似之处。第三个证据是通过测量肿瘤生长速度获得的。胶质母细胞瘤是一种侵袭性疾病,部分原因是它是不可预测的:当将异质性癌细胞分别注射到模型动物体内时,一些动物体内的癌细胞会处于休眠状态,而另一些动物体内的活性肿瘤会迅速发展。这是有道理的,因为作为人类,我们可以在年老时平静地死去,而不知道我们有这种休眠的肿瘤。然而,在实验室的培养皿中,所有的肿瘤都以同样的速度生长和扩散。在我们的3d生物打印肿瘤中,这种异质性保持不变,发展过程与我们在患者或动物模型中看到的广谱相似。”
据萨奇-法纳罗教授说,这种创新的方法还将以比现在快得多的速度开发新药物,以及发现新的药物靶点。希望在未来,这项技术可以为病人提供个性化的医疗服务。
“如果我们从病人的组织中提取样本,以及它的细胞外组织矩阵,我们可以从这100个微小肿瘤样本中提取3d生物打印,并在不同的组合中测试许多不同的药物,以发现这种特定肿瘤的最佳治疗方法。另外,我们可以在3d生物打印肿瘤上测试多种化合物,并决定哪一种是最有潜力的进一步开发和投资的潜在药物。但也许最令人兴奋的方面是在癌细胞中找到新的可药物作用的靶蛋白和基因——当肿瘤位于人类病人或模型动物的大脑中时,这是一项非常困难的任务。我们的创新为我们提供了前所未有的机会,没有时间限制,更好地模拟临床场景的3D肿瘤,实现了最佳的研究。”
受欢迎的文章










 罗尼特·萨奇-法纳罗教授,他领导的团队开发了3d生物打印胶质母细胞瘤模型
罗尼特·萨奇-法纳罗教授,他领导的团队开发了3d生物打印胶质母细胞瘤模型