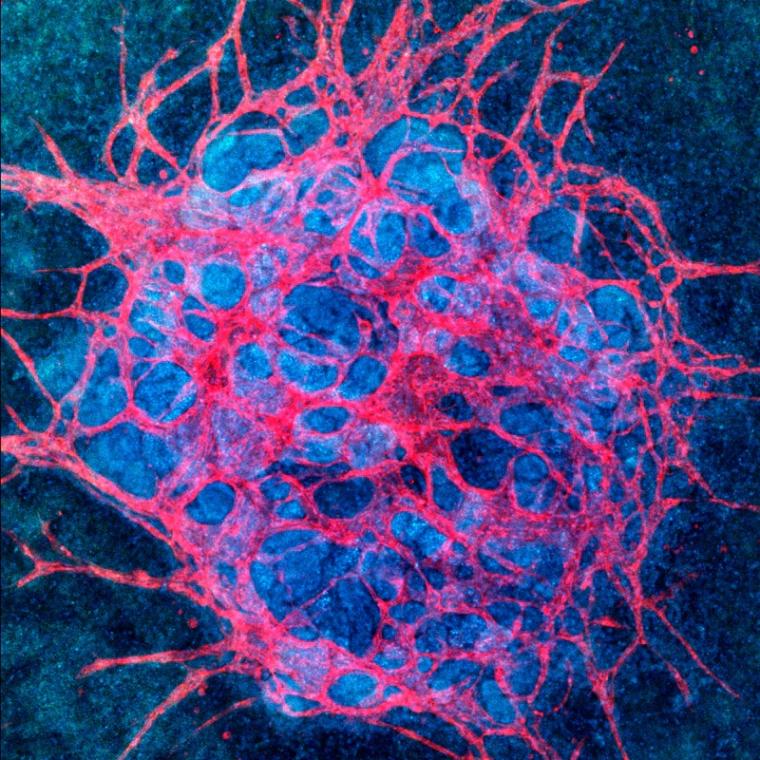
近年来,研究人员在培养皿中创造出了被称为类器官的微型器官,其中包含了人体器官中发现的许多细胞类型和复杂的微结构,如肾脏、肝脏、肠道,甚至大脑。然而,大多数体外培养的类器官缺乏所需的脉管系统,以提供氧气和营养,清除代谢废物,并促进不同类型细胞之间的沟通,推动它们成熟为真正的功能性组织构件。
对于肾脏类器官,这一缺陷使研究人员无法在体外模拟肾脏的关键功能,包括血液过滤、再吸收和尿液产生。创建强大的血管化肾类器官可以更好地模拟肾脏疾病,增强肾药物毒性测试,并最终导致肾脏替代疗法的新基石。
现在,来自威斯生物工程研究所、哈佛保尔森工程与应用科学学院(SEAS)、布莱根妇女医院的一个研究小组,Jennifer Lewis和Ryuji Morizane领导的哈佛干细胞研究所开发了一种强大的新方法,作为该研究所新的3D器官工程计划的一部分。与以前的静态培养方法相比,通过将干细胞衍生的类器官暴露在流体剪切应力下,他们能够显著扩大类器官衍生的血管网络,并改善肾脏隔室的成熟。
2015年,Ryuji Morizane和Joseph Bonventre开发了一种方法,使他们能够从人类多能干细胞中获得3D肾脏类器官。“虽然我们的类器官和其他实验室产生的类器官含有大量组织良好的肾元和原始血管,但它们仍然缺乏具有可灌注腔的广泛性血管腔室,”通讯作者Morizane,医学博士,布里格姆妇女医院和哈佛医学院(HMS)的助理教授说。
最近,世界各地的研究人员通过将肾脏器官移植到动物体内,使其成熟,从而与宿主体内的脉管系统相连接。Morizane说:“我们的研究首次证明,通过将生长中的类器官暴露在液体流动中,这是一种已知对人体组织发育起重要作用的机械线索,我们可以极大地增强它们的血管化和体外成熟。”
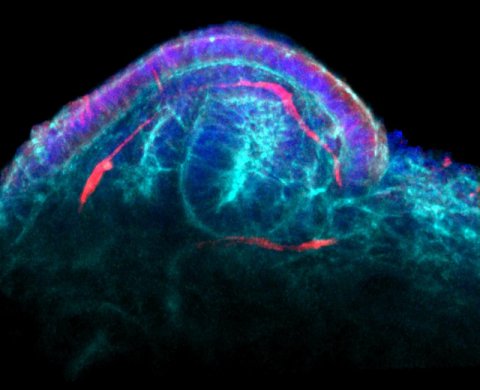
为了完成这一壮举,该团队使用了来自刘易斯实验室的专业技术,该实验室在创建血管化人体组织方面具有开创性的策略,包括3D芯片上的肾脏模型,使用3D生物打印,可以灌注并持续很长时间。基于这些发现,他们假设液体流动也可以促进生长中的肾脏类器官中前体内皮细胞形成血管。
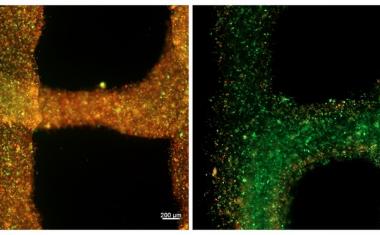
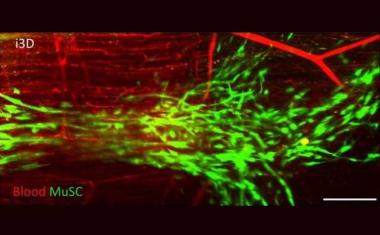
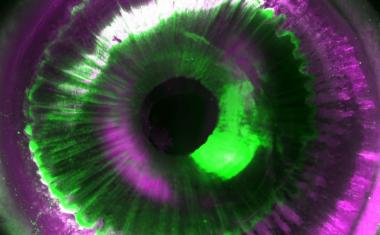
Kimberly Homan博士和Navin Gupta医学博士是这项研究的第一作者,他说:“我们确定了细胞外基质、介质添加剂和流体剪切应力的正确组合,在这种情况下,人类干细胞衍生的类器官在我们的3d打印微流控芯片中生长会蓬勃发展。”Gupta补充道:“血管网络在上皮结构附近形成,形成肾小球和管状室,反过来促进上皮细胞的成熟。这个整合的过程就像一条双行道。”霍曼是维斯研究所(Wyss Institute)和SEAS的刘易斯小组的研究助理,古普塔(Gupta)是布里格姆研究所(Brigham)莫里桑团队的临床研究员。
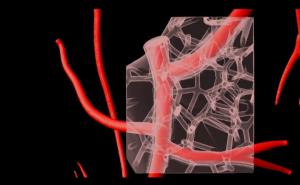
生长在3d打印芯片上的血管与开放腔形成了一个相互连接的网络,可以灌注液体,通过直接成像荧光珠在其中自由移动来确认。霍曼说:“我们很兴奋地看到,这些血管化的肾小球和管状结构在体内的正常肾脏发育过程中经历了相同的阶段。”
”这一重要发展开辟了新的途径,准确地检测药物毒性体外分化的肾元隔间和建模肾脏疾病,如多囊肾疾病,影响特定结构和细胞类型使用patient-derived干细胞作为起点,“共同通讯作者刘易斯说,科学博士cari jo clark。他是维斯研究所的核心教员,也是其3D器官工程计划的共同领导者。“我们的方法可能为其他类型的类器官血管化铺平道路,如肝脏类器官。”刘易斯也是海洋工程学院的Hansjörg Wyss生物启发工程教授。
“这项研究是机械生物学的重要性和维斯研究所3D器官工程计划的潜在力量的一个很好的例子。它为许多旨在为研究、制药和组织再生应用创造功能性人体组织的努力提供了重要的基石。”
来源:哈佛大学