如果在人类中得到证实,这些新的心脏瓣膜可以防止每年成千上万出生的先天性心脏缺陷儿童重复进行瓣膜置换手术。这些瓣膜还可以保存至少6个月,这意味着它们可以为外科医生提供一个“现成”的治疗选择。
“这是儿科心脏研究向前迈出的一大步,”这项研究的高级研究员、明尼苏达大学生物医学工程系、化学工程和材料科学系教授罗伯特·特兰奇洛(Robert礠拉吉罗)说。“这是首个将瓣膜植入大型动物模型的实验,在我们的实验中是一只羊羔,它可以和动物一起成长到成年。我们还有很长的路要走,但这让我们在未来儿童临床试验的道路上走得更远。我们对未来几年实现这一目标的可能性感到兴奋和乐观。”
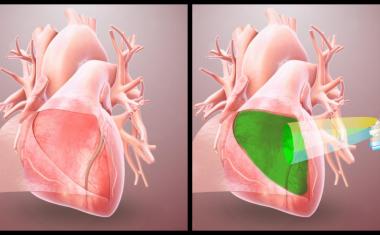
目前,研究人员还无法为儿科患者开发出一种能够生长和维持功能的心脏瓣膜。对于这些有心脏缺陷的儿童,唯一被接受的选择是用经过化学处理的动物组织制成的瓣膜。这些瓣膜通常会因钙化而功能失调,需要更换,因为它们不能随儿童一起生长。这些儿童通常需要忍受五次(或更多)的开胸手术,直到成年后植入机械瓣膜。这就要求他们的余生都要服用血液稀释剂。
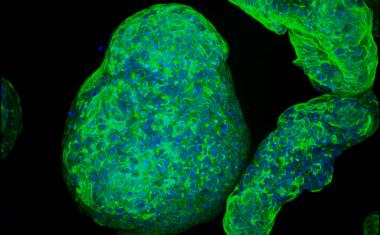
在这项研究中,特兰奎略和他的同事使用了一种混合的组织工程和再生医学来制造生长中的心脏瓣膜。在8周的时间里,他们使用了一种专门的组织工程技术,在实验室里从出生后捐赠者的皮肤细胞中产生了血管状的管子。为了研制这种试管,研究人员将捐赠的绵羊皮肤细胞与一种叫做纤维蛋白的凝胶状物质结合在一起,形成试管,然后使用生物反应器提供细胞生长所必需的营养物质。
然后,研究人员使用特殊的洗涤剂将所有绵羊细胞从组织状管中洗去,留下一个在植入时不会引起免疫反应的无细胞胶原基质。这意味着试管可以储存和植入,而不需要使用接受者的细胞定制生长。
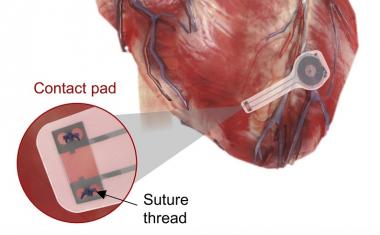
下一步是将三根这样的管子(直径约16毫米)精确地缝合在一起,形成一个封闭的环。然后,研究人员稍微修剪它们,制造出瓣叶,复制出一个直径约19毫米的类似心脏瓣膜的结构。
“经过这些最初的步骤,它看起来像一个心脏瓣膜,但接下来的问题是,它是否能像心脏瓣膜一样工作,是否能生长,”特兰奇洛说。“我们的发现证实了这两点。”
第二代三管瓣膜植入三只羔羊的肺动脉。52周后,瓣膜的基质被来自受体羔羊的细胞所填充,瓣膜的直径从19 mm增加到生理正常的25 mm左右。研究人员还发现,根据超声图像测量,瓣叶的长度增加了17%到34%。此外,研究人员还发现,三管瓣膜比现有的动物瓣膜工作得更好,几乎没有钙化或血液凝固,而其他瓣膜在移植到相同年龄的羊羔身上后显示出这种情况。
“我们从之前的研究中知道,工程管道具有再生和生长的能力,但最大的挑战是如何保持传单功能的生长阀门管道,在一年经历4000万次循环。”这项研究的首席研究员、特兰奇洛实验室的明尼苏达大学高级研究员Zeeshan Syedain说。“当我们看到从小羊羔到成年绵羊的瓣膜在整整一年的时间里功能良好时,这是非常令人兴奋的。”
安静地说,下一步是tri-tube阀直接植入心脏右心室模拟最常见的外科修复的过程,然后开始请求批准美国食品和药物管理局(FDA)进行人体临床试验在未来几年。
“如果我们有一天能让这些瓣膜被批准用于儿童,这将对患有心脏缺陷的儿童和他们的家庭产生巨大的影响,他们必须应对多次手术的巨大压力,”特兰奇洛说。“我们有可能将这些孩子需要忍受的手术次数从五次减少到一次。这是梦想。”
这项研究发表在科学转化医学.阀门制造程序也获得了明尼苏达大学初创公司Vascudyne公司的专利和许可。
来源:明尼苏达大学