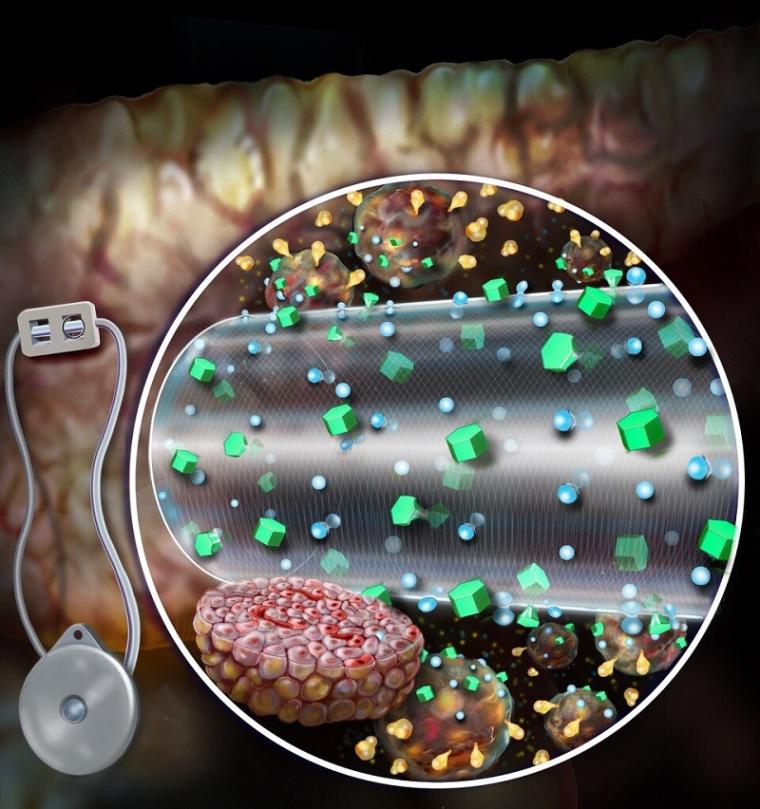
全世界有4000多万人受艾滋病影响1型糖尿病(T1D)自身免疫性疾病胰岛素胰腺中产生β细胞的细胞被免疫系统破坏。今天,有几种新的和新兴的1型糖尿病治疗方法糖尿病包括宏观封装装置(MEDs)——设计用于容纳和保护胰岛素分泌细胞的隔间。就像骑士身上的一套盔甲,药物可以保护体内的细胞免受攻击(来自宿主免疫系统),同时允许营养物质进出,使细胞能够继续存活。但是药物有一些局限性,扩大这种设备在人类中的应用一直是一个挑战。
来自布里格姆妇女医院的一组研究人员与哈佛大学和马萨诸塞大学医学院的同事合作设计了一种对流增强MED (ceMED),它可以持续地将细胞沐浴在它们需要的营养中,提高细胞承载能力,同时提高细胞存活率,葡萄糖敏感性和及时分泌胰岛素。在临床前的模型中,ceme在植入后两天内对血糖水平迅速做出反应。
通讯作者杰夫·卡普博士说:“由于最近的进展,我们越来越接近于拥有一种无限来源的β样细胞,这种细胞可以通过分泌胰岛素对葡萄糖作出反应,但下一个挑战是以一种微创的方式将这些细胞导入体内,并具有最大的功能和长寿性。”。,临床麻醉学、围手术期和疼痛医学的主要研究者和杰出主席。“我们的设备在移植后显示出增强的细胞活力和最小的延迟。这是该系统的一个强有力的临床前概念证明。”
目前的med是扩散依赖的——营养物扩散穿过设备的外膜,只有少数细胞可以接受营养物和氧气,并反过来分泌胰岛素。ceMED的设计目的是通过连续流动的液体向被封装的细胞提供对流营养,允许多层细胞生长和生存。该团队的原型有两个室,一个是平衡室(EqC),收集周围环境的营养物质,另一个是细胞室(CC),容纳受保护的细胞。EqC包裹在聚四氟乙烯中,聚四氟乙烯是一种具有允许液体进入的孔隙的半透膜。CC周围的额外内膜选择性地允许营养物质运输和保护免受免疫反应。灌注液体流经多孔中空纤维到达CC,其营养浓度与植入物周围组织相似。中空纤维允许胰岛素和葡萄糖自由通过,但不允许关键免疫分子攻击被包裹的细胞。
合著者道格·梅尔顿博士说:“应用干细胞衍生的胰岛治疗自身免疫性或1型糖尿病现在已经发展到寻找一种方法来保护细胞免受免疫排斥,并在移植后最大限度地提高其存活率和功能。”。,哈佛干细胞研究所干细胞和再生生物学系的教授。“对流增强型宏封装可能是实现所有这些目标的可行方法。”
推荐文章
与传统的胰岛素泵相比,该设备有许多优点,允许细胞按需分泌胰岛素,并在血糖水平下降时迅速停止分泌胰岛素。在1型糖尿病鼠模型中,ceMED可以提高细胞的存活率和胰岛素分泌,并在移植后2天开始降低血糖水平。
“ceMED装置有可能成为一个自动系统,不需要不断地重新填充和更换胰岛素筒,”主要作者Kisuk Yang博士说,他曾是Karp实验室的博士后研究员,现在是韩国仁川国立大学生物工程系的教员。
“由于其响应性,这种设备和新型的血流增强方法可能对‘脆性’糖尿病患者特别有用,这些患者的糖尿病导致血糖水平不可预测的波动,”Eoin O' cebhaill博士(现就职于爱尔兰都柏林大学)补充道。Eoin O' cebhaill博士是该研究的合著者,在卡普实验室做博士后时帮助开发了这一概念。该团队指出,将该设备带到临床需要探索的未来方向,包括扩大细胞装载能力和优化供人使用的灌注流系统。
“总的来说,这些结果突出了ceMED相对于现有扩散型设备的显著优势,包括提高了细胞存活率,减少了纤维包裹,随着时间的推移会损害功能,以及更快的胰岛素分泌开/关速率,”Karp说。“这种方法有可能提高β细胞替代疗法的成功率,以帮助许多T1D患者及其家属应对这一具有挑战性的疾病。”
研究结果发表在《美国国家科学院院刊》上。
来源:布里格姆妇女医院