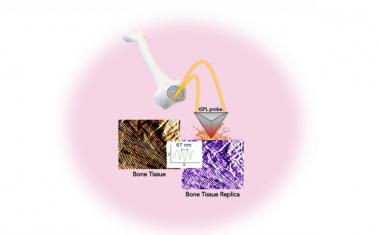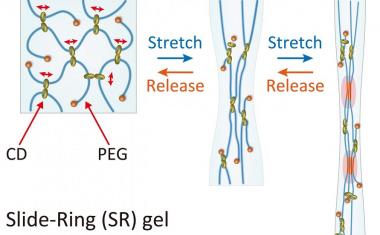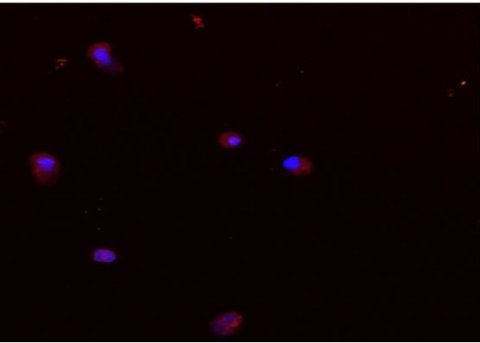
一个由物理学家,化学家和组织工程专家们使用了特别设计的黄金纳米粒子“寻找”特定的人体骨骼干细胞-产生荧光光来显示它们在其他类型细胞中的存在,并允许它们被分离或“富集”。研究人员得出结论,他们的新技术比其他方法更简单、更快,在富集干细胞方面的效率是其他方法的50-500倍。
这项研究由肌肉骨骼科学教授理查德·奥瑞佛和美国农业部的安东尼奥斯·卡纳拉斯教授领导量子,物理与天文学院光与物质组,已发表于ACS Nano.
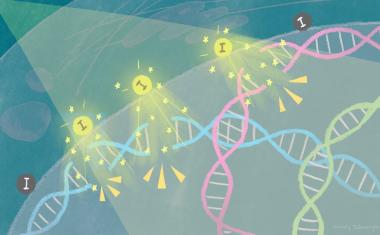
在实验室测试中,研究人员使用金纳米颗粒——由数千个金原子组成的微小球形颗粒——包裹着寡核苷酸(DNA链),以光学方式检测骨髓中骨骼干细胞的特定信使RNA (mRNA)特征。当检测发生时,纳米粒子会释放荧光染料,使干细胞在显微镜下与周围的其他细胞区别开来。然后,干细胞可以使用复杂的荧光细胞分选过程分离。
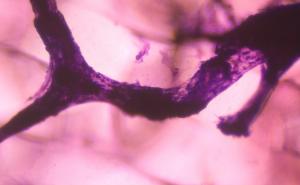
干细胞是尚未特化的细胞,可以发育成不同的功能。鉴定骨骼干细胞可以让科学家在特定的条件下培养这些细胞,以促进骨骼和软骨组织的生长和形成——例如,帮助修复骨折。
人口老龄化带来的挑战之一是需要新颖的、经济有效的骨修复方法。全球有三分之一的女性和五分之一的男性有患骨质疏松性骨折的风险,这一成本是巨大的,仅骨折每年就给欧洲经济造成170亿欧元的损失,给美国经济造成200亿美元的损失。
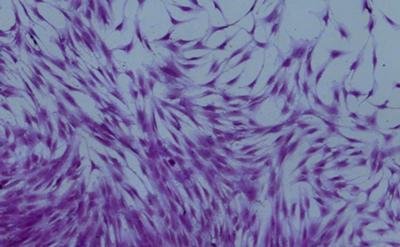
在南安普顿大学的骨骼和联合研究小组中,Oreffo教授和他的团队已经研究了超过15年的骨干细胞疗法,以了解骨组织的发展,并生成骨骼和软骨。与此同时,Kanaras教授和他的同事们一直在设计新型纳米材料,并研究它们在纳米材料领域的应用生物医学科学和能源。这项最新的研究有效地将这些学科结合在一起,是合作和跨学科工作所能带来的影响的典范。
Oreffo教授说:“基于骨骼干细胞的治疗为老年人群的骨病治疗和骨再生医学提供了一些最令人兴奋和最有前途的领域。目前的研究已经从我们认为会丰富骨骼干细胞的目标中提取了独特的DNA序列,并且,使用荧光激活细胞排序(FACS),我们已经能够丰富患者的骨骼干细胞。识别独特的标记是骨干细胞生物学的圣杯,虽然我们还有一段路要走;这些研究为我们定位和识别人类骨干细胞的能力以及其令人兴奋的治疗潜力提供了一步改变。”
Oreffo教授补充说:“重要的是,这些研究显示了跨学科研究的优势,以解决与最先进的分子/细胞生物学相结合的挑战性问题纳米材料“化学平台技术。”
卡纳拉斯教授说:“材料的适当设计对于它们在复杂系统中的应用至关重要。定制纳米粒子的化学性质,我们就能在它们的设计中设定特定的功能。
“在这个研究项目中,我们设计了纳米颗粒包裹短序列DNA,能够感知骨骼干细胞中的HSPA8 mRNA和Runx2 mRNA,并结合先进的FACS门控策略,以实现来自人类骨髓的相关细胞的分类。
纳米材料设计的一个重要方面涉及到调控纳米颗粒表面寡核苷酸密度的策略,这有助于避免细胞内DNA的酶降解。对寡核苷酸的荧光报告使我们能够在实验的不同阶段观察纳米颗粒的状态,确保细胞内传感器的质量。”
导致研究人员也承认,成就都可能由于工作的经验丰富的研究员和博士生参与这项研究以及与汤姆布朗教授和博士合作Afaf E-Sagheer牛津大学的多种功能性寡核苷酸的合成。
科学家们目前正在将单细胞RNA测序应用于平台技术,该技术是与牛津大学和南安普顿生命科学研究所(IfLS)的合作伙伴共同开发的,以进一步提炼和丰富骨干细胞,并评估其功能。该团队提议将临床应用与临床前骨形成研究,以产生概念研究的证据。
来源:南安普顿大学