通过破坏基因信息(RNA)而不是潜在基因(DNA),研究人员可以研究那些以前可能很难或不可能操纵的基因,因为它们对生命至关重要,或涉及生物发展的关键阶段。这种方法还允许靶向母亲贡献的基因rna,这些基因rna沉积在卵子中,启动最早的遗传程序。
该研究确定了CRISPR-Cas技术以特定和系统的方式靶向胚胎动物模型中的RNA研究结果表明,该技术可以应用于广泛的水生和陆生模型,包括斑马鱼、青鳉鱼、鳉鱼和老鼠。“这项研究令人兴奋的地方不仅在于我们发现了什么,还在于我们能做什么,”斯托尔斯研究所助理研究员、该研究的联合负责人Ariel Bazzini博士说。“我们仍然不明白基因是如何在发育的最初阶段启动的。现在,我们可以通过靶向它们的RNA信息,一个接一个地找出答案。”
“我们也对这项技术的低成本感到非常兴奋,”Bazzini说。“任何研究斑马鱼或其他动物胚胎的实验室都可以使用这种方法。事实上,我们已经将试剂和方案分发给了世界各地的几个实验室。”
在发育开始之前,卵子必须首先与精子相遇。由此产生的胚胎一半来自母亲,一半来自父亲。除了基因组外,胚胎还含有母亲提供的RNA和蛋白质等成分。巴兹尼说:“母亲的贡献是一个我们许多人都想解开的谜。”。然而,在斑马鱼(许多发育生物学家选择的模式生物)中系统地靶向RNA的尝试却没有成功。被恰当地命名为RNA干扰的方法已经成为基因功能研究的主流,但在斑马鱼或其他鱼类或青蛙身上不起作用。使用合成遗传密码条的其他方法称为吗啉或反义寡核苷酸,有时与毒性和靶向效应有关。
因此,当巴兹尼和他的合作者、朋友、帕布罗·德·奥拉维德大学教授米格尔·莫雷诺·马特奥斯博士注意到有报道称CRISPR技术已被用于降解酵母、植物和哺乳动物细胞中的RNA时,他们急切地想尝试一下。Moreno Mateos与Bazzini同时是耶鲁大学Antonio Giraldez实验室的博士后,被认为是体内CRISPR Cas技术优化方面的专家。
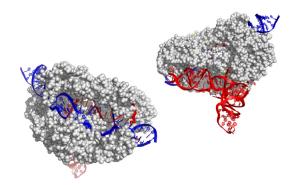
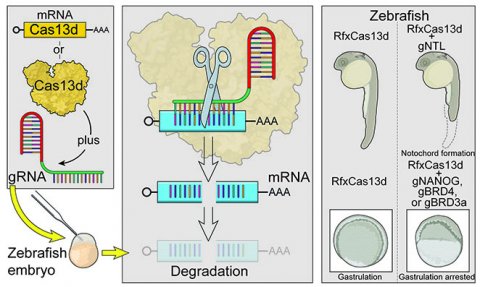
CRISPR-Cas13系统依赖于两种成分——一种称为“引导”RNA的短RNA序列和一种称为Cas13(Cas的一部分,或CRISPR相关的蛋白质家族)的酶,该酶切割细胞中可能排列并结合到该引导序列的任何RNA信息。研究人员测试了四种不同的Cas13蛋白,这些蛋白在以前的研究中已经成功使用。他们发现,除了一种叫做RfxCas13d的蛋白质外,Cas13蛋白质对发育中的斑马鱼要么低效,要么有毒。
然后,他们检测了在斑马鱼胚胎中以CRISPR-RfxCas13d为靶点的RNA是否会产生与改变该生物体的潜在DNA相同的缺陷。例如,当他们以tbxta基因的RNA为目标时,斑马鱼胚胎是无尾的。tbxta基因是长尾所必需的。
研究人员继续证明CRISPR系统可以有效地靶向多种RNA,包括母亲提供的RNA和胚胎产生的RNA,使RNA水平平均降低76%。Stowers内外的合作者帮助得出了这一统计数据,并表明该技术也适用于killifish、medaka和小鼠胚胎。“CRISPR-RfxCas13d系统是一种高效、特异和廉价的方法,可以全面用于动物胚胎,”该研究的共同负责人莫雷诺·马特奥斯说。“有了这个工具,我们将有助于理解生物学和生物医学的基本问题。”
研究人员希望研究的一个基本问题是RNA在发育早期所起的作用。母亲留下的RNA必须在胚胎基因组上线的同时被移除;否则,胚胎永远不会发育。巴兹尼说:“我们认为,这一工具可以对我们对不孕症和发育问题的理解产生深远的影响。”。
这项研究发表在杂志上发育细胞。
资料来源:美国密苏里州斯托瓦斯医学研究所