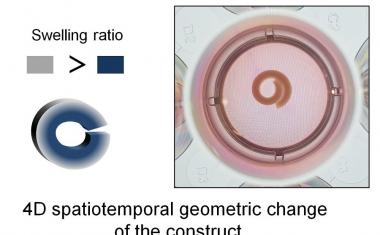
用实验室制造的组织来修复或替换受损的组织器官是对未来医学的伟大设想之一。合成材料可以作为脚手架吗组织因为,与自然组织不同,它们在生物体中保持稳定足够长的时间,使身体形成新的自然结构。功能性组织的一个基本要求是,血管必须能够在组织中生长,并与有机体的血管系统相连,这样组织才能获得适当的氧气和营养。然而,到目前为止,几乎还不知道是哪种物质特性促进了血管的生长。
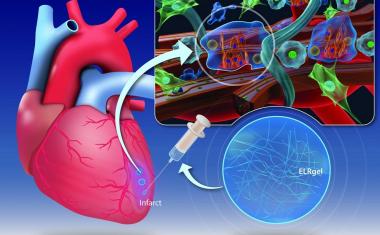
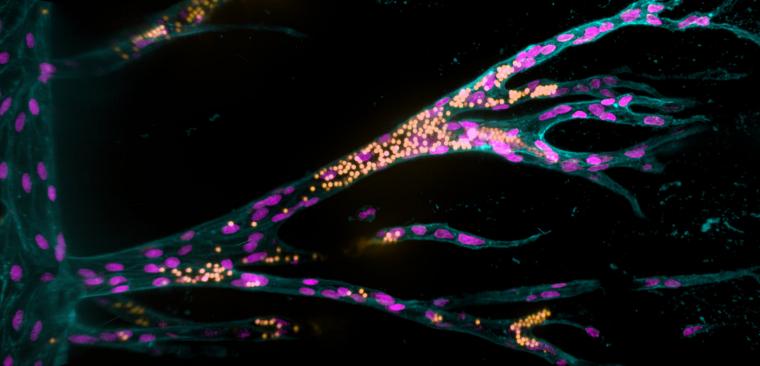
由德国马克斯·普朗克分子生物医学研究所(Münster)生物医学工程师布雷塔·特拉普曼博士领导的团队开发了一种细胞培养系统,该系统首次能够在由合成材料制成的框架内生长出功能性血管系统。科学家们,在一个特别的水凝胶它们的特性可以通过一种可控的方式改变,首先从人体血管内衬细胞中培育出一根母血管。然后他们研究了人工细胞环境的材料特性如何影响附加物质的形成血管并调整它们。
在总结关键发现时,Trappmann强调:“合成的组织材料必须激活血管细胞细胞膜上的某些粘附分子,以便细胞成群地从母血管迁移并形成管状结构。同时,材料必须能够充分降解,细胞才能形成足够大小的血管”。
为了模拟细胞的自然环境,许多额外的生物分子和细胞必须在随后的步骤中集成到模型系统中——这些可能是信号蛋白、免疫细胞或稳定血管的细胞。特拉普曼解释说:“此外,所有这些因素的影响都与自然组织有关,而且每个器官的影响都不同。”她说,了解所有这些是一个长期的目标,但最终,这些知识可能会被用于种植植入式组织。
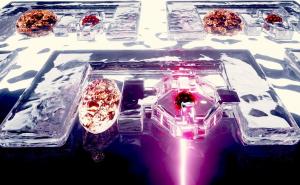
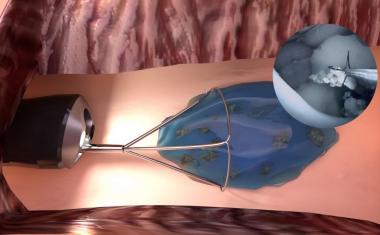
由水凝胶制成的3D组织框架
在这项研究中,研究人员完善了Trappmann在美国波士顿大学和哈佛大学做博士后期间与同事开发的一个模型系统。它由一种三维糖基水凝胶组成,科学家们用针灸针在其中制造了两个通道。每个通道的直径为400微米,它们彼此平行,距离约为1毫米。在一个通道中,科学家们将内皮细胞植入自然组织的血管中。Trappmann解释说:“内皮细胞相互接触,并附着在通道内的合成组织环境中,这样大约一天后就形成了一条母血管。”当这种情况发生时,科学家们将一种分子混合生长因子通过第二通道在自然组织中驱动血管生长,然后内皮细胞迁移到水凝胶中。
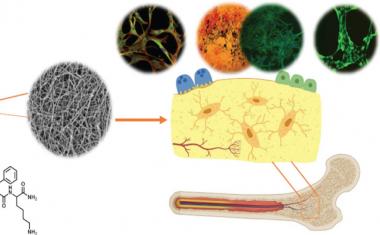
分子使血管在运动中形成
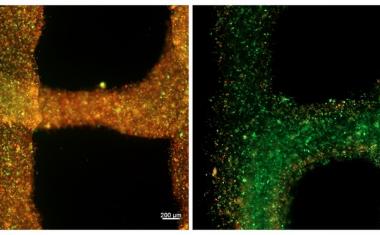
然后,科学家们想要找出水凝胶的哪些特性决定迁移的内皮细胞是否真的会形成新的血管。他们研究了细胞膜中所谓的粘附分子的激活所起的作用,细胞通过这些分子附着在周围环境中。研究人员首先用不同数量的多肽丰富了水凝胶组织框架,这些多肽可以激活内皮细胞膜上发现的一种叫做整合素的黏附分子。肽浓度越高,内皮细胞通过水凝胶迁移的越多。
相反,当科学家阻断整合素的功能时,他们观察到细胞只是单独迁移。在进一步的步骤中,该团队研究了这一过程,观察了两个特定的整合素亚型。Trappmann说:“我们发现整合素αvβ3是内皮细胞群体迁移必须被激活的关键粘附分子。”科学家们还表明,细胞集体迁移反过来也是内皮细胞形成连接到母血管的腔体的先决条件。
细胞必须能够自由移动
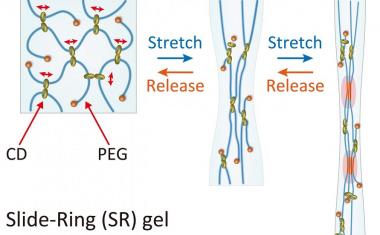
尽管这些血管细胞形成了管状结构,但它们比自然组织中的血管细胞要小。科学家们推测,这可能是因为合成水凝胶比天然组织更难降解,而且细胞可以通过的孔更小。由于水凝胶由特定分子交联的糖分子链组成,科学家们的解决方案是交换这些交联分子,这样细胞就可以利用它们释放的酶更快地裂解水凝胶。这使得细胞迁移得更快,形成更大的血管结构。
这项研究发表在自然通讯.