非酒精性脂肪肝(NAFLD)是全球最常见的慢性肝病。发达国家30%的人患有该病,美国约25%的人患有该病。该疾病的危险因素包括肥胖、糖尿病、高胆固醇和不良饮食习惯,但这并不排除没有这些危险因素的个人。
肝脏中通常有少量脂肪;然而,如果脂肪量占肝脏的5%或更多,就被认为是NAFLD,必须设法避免严重的疾病进展。在最坏的情况下,NAFLD可导致肝脏肿胀和炎症、纤维化或结疤、肝衰竭或肝癌。
肝脏是一个复杂的器官,NAFLD进展所涉及的生理事件涉及肝脏中发现的多个步骤和不同种类的细胞。肝脏中脂肪酸的异常积累会触发免疫细胞库普弗细胞(Kupffer cells),以及肝脏血管内壁的内皮细胞,释放信号和化学反应分子。这些分子刺激称为星状细胞的细胞合成并沉积纤维化蛋白,从而导致肝脏瘢痕形成。
NAFLD可以通过健康的饮食和运动以及减肥和/或控制体重来控制,但目前尚无确切的治疗方法。开发治疗方法的主要困难之一是没有准确的NAFLD模型来测试治疗效果。动物模型不能真正代表人类NAFLD的步骤,过去开发的人类模型也显示出局限性。一个相对先进的“人工纤维化模型”已经建立,用于刺激疾病序列的最终纤维化发展部分,但它与观察到的完整疾病进展没有完全相关性。
Terasaki生物医学创新研究所(TIBI)的一个合作团队开发了一种先进的、多细胞的、具有结构代表性的芯片上肝脏模型,该模型模拟NAFLD的整个进展序列。该模型包含参与该序列的四种人类原代细胞:库普弗细胞、内皮细胞、星状细胞和肝细胞。
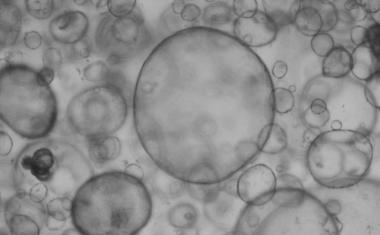
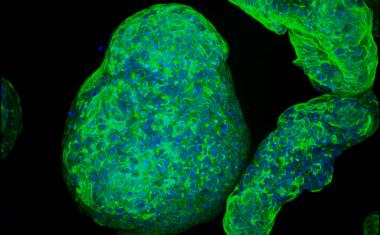
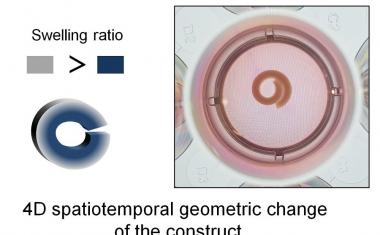
这些细胞混合在一起,在一排金字塔形微孔中作为多细胞微组织生长;调整细胞数量和比例,以产生最佳形状的微组织,以维持与天然肝组织相似的营养和氧气浓度。然后将微组织包裹在凝胶物质内,使组织更充分地匹配天然肝组织的结构和细胞间相互作用。
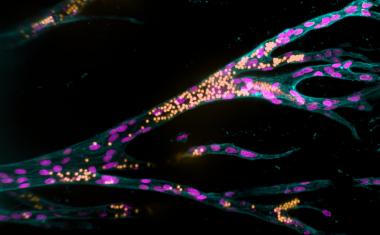
该团队在旨在验证星状细胞在NAFLD中的作用的试验中使用了他们的多细胞芯片肝脏模型。他们得出的结论是,星状细胞似乎与血管的形成、化学反应性化合物的产生以及某种程度上脂肪酸的积累有关。他们还得出结论,星状细胞可能与Kupffer和其他肝细胞相互作用,产生特定的信号分子。所有这些事件都是NAFLD完全进展的关键因素。
“我们的芯片上多细胞肝脏系统是一个实验室模型,比以前的模型更先进,更充分地反映了NAFLD的自然进展。”
研究小组还测试了在他们的模型中加入脂肪酸的效果。结果表明,脂肪酸和活跃的星状细胞的存在加速了炎症反应,增加了纤维化蛋白的产生,进一步验证了模型对NAFLD自然进展的模拟。
随后的试验比较了TIBI的NAFLD模型和前面提到的由转化生长因子(TGF)-β驱动的人工纤维化模型。在比较两种模型时,TIBI的纤维化模型模拟了NAFLD的自然进展,表现出比人工纤维化模型更高的脂肪积累和纤维化分子水平。
此外,研究小组在两种模型中测试了抗纤维化药物的反应。试验表明,TIBI的NAFLD模型在药物递送时表现出更强的药物转运和代谢反应。这一发现对于筛选治疗NAFLD的潜在药物具有重要意义。
TIBI团队成员Junmin Lee博士说:“我们的芯片上多细胞肝脏系统是一个实验室模型,比以前的模型更先进,更充分地反映了NAFLD的自然进展。”“这得到了我们比较研究的实验结果的支持。”
希望TIBI的NAFLD模型可以用于阐明这种疾病背后的机制,并测试可能的药物治疗的疗效。它还具有个性化治疗的潜力,可以从单个患者获得所需的全部细胞阵列,并使用它们创建定制的疾病模型。
Terasaki研究所所长兼首席执行官Ali Khademhosseini博士说:“这里描述的多细胞模型是我们在开发个性化生理模型方面所做工作水平的示范。”。“它有可能帮助发现一种流行且可能致命的疾病的治疗方法。”
来源:寺崎研究所