存在的威胁新型冠状病毒肺炎强调迫切需要开发针对新出现的健康威胁的有效疗法。其中一个奢侈品深度学习只要我们能跟上病毒的威胁,并获取正确的数据,我们就有能力在事态发展的过程中改变现状。
与所有新的医学疾病一样,数据往往需要时间来掌握,而病毒不需要时间来放慢速度,这带来了一个艰巨的挑战,因为它可以迅速变异,并对现有药物产生耐药性。这导致了麻省理工学院计算机科学和人工智能实验室(CSAIL)和贾米尔诊所机器学习要问的问题是:我们如何为迅速蔓延的疾病确定正确的协同药物组合SARS-CoV-2?
通常情况下,数据科学家利用深度学习技术,利用现有的大型数据集挑选出治疗癌症和心血管疾病的药物组合,但可以理解的是,它们不能用于数据有限的新疾病。
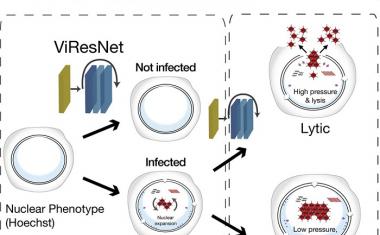
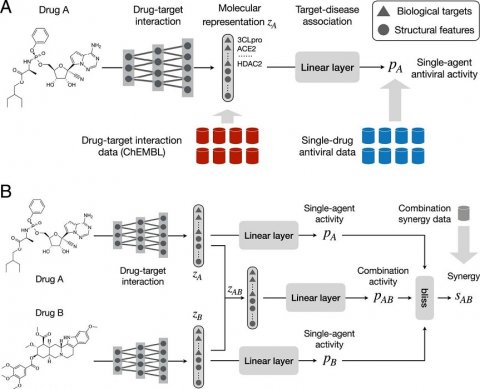
没有必要的事实和数据,团队需要一种新的方法:a神经网络他身兼两职。由于药物协同作用通常通过抑制生物靶标(如蛋白质或核酸)发生,该模型联合学习药物-靶标相互作用和药物-药物协同作用来挖掘新的药物组合。药物靶点预测器对药物和一组已知的与所选疾病相关的生物靶点之间的相互作用进行建模。目标-疾病关联预测器学习了解药物的抗病毒活性,这意味着确定感染组织培养中的病毒产量。它们一起可以预测两种药物的协同作用。
发现了两种新药组合:瑞德西韦(remdesivir,目前已获FDA批准用于治疗COVID-19)和利血平,以及瑞德西韦和IQ-1S,在生物试验中证明,它们对病毒具有强大的抗作用。
“通过模拟药物和生物靶点之间的相互作用,我们可以显著减少对联合协同效应数据的依赖,”中国科学技术学院(CSAIL)博士、麻省理工学院布罗德研究所(MIT Broad Institute)博士后金文功说,他是这项研究的一篇新论文的第一作者。“与之前使用药物-靶点相互作用作为固定描述符的方法不同,我们的方法学会了从分子结构预测药物-靶点相互作用。这是有利的,因为大部分化合物具有不完全的药物-靶点相互作用信息。”
使用多种药物以最大限度地发挥药效,同时减少副作用,在上述癌症和心血管疾病,包括肺结核、麻风病、疟疾等许多其他疾病中几乎无处不在。非常重要的是,由于许多耐药突变是相互排斥的,使用专门的鸡尾酒药物可以减少严重的、有时是公共的耐药性威胁(想想耐甲氧西林金黄色葡萄球菌,称为“MRSA”)。对于一个病毒来说,同时产生两种突变,然后在联合治疗中对两种药物产生抗药性要困难得多。
该模型也不局限于SARS-CoV-2——它也可以用于传染性日益增强的delta变种。要把它扩展到那里,你只需要额外的药物联合增效数据来研究突变。该团队还将他们的方法应用于艾滋病和胰腺癌。
为了进一步完善他们的生物模型,该团队计划加入更多的信息,如蛋白质相互作用和基因调控网络。
他们正在探索的另一个未来工作方向是“主动学习”。由于药物组合的尺寸有限,许多药物组合模型都偏向于特定的化学空间,因此预测存在很大的不确定性。主动学习有助于指导数据收集过程,并在更广阔的化学空间中提高准确性。
这项研究发表在美国国家科学院院刊(PNAS)。
来源:麻省理工学院