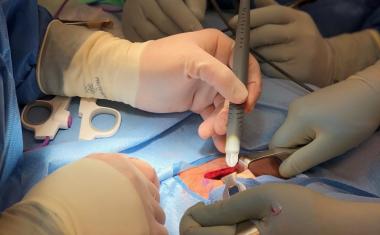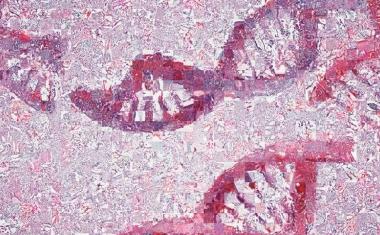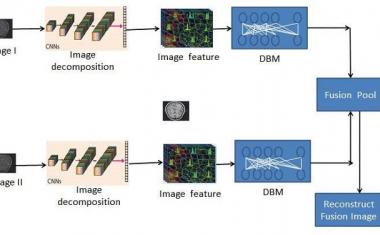
虽然显微技术能够以高空间细节研究生物过程,但它们只允许对分子标记进行有限的测量。这些都是用从组织中提取的蛋白质或DNA来确定的。因此,空间细节是不可能的,这些标记和微观结构之间的关系通常是不清楚的。“我们知道,在乳腺癌的病例中,肿瘤组织中迁移的免疫细胞,即淋巴细胞的数量对患者的预后有影响。也有关于这个数字是否有预测价值的讨论——换句话说,它是否能让我们说一种特定的治疗有多有效,”Charité病理研究所的Frederick Klauschen教授说。
“我们面临的问题是:我们有良好和可靠的分子数据,我们有良好的高空间细节的组织学数据。我们还没有得到的是成像数据和高维分子数据之间的决定性联系,”克劳斯-罗伯特博士补充道,Müller机器学习在你柏林。这两名研究人员已经在位于柏林工业大学的国家人工智能卓越中心——柏林学习和数据基础研究所(BIFOLD)合作多年。
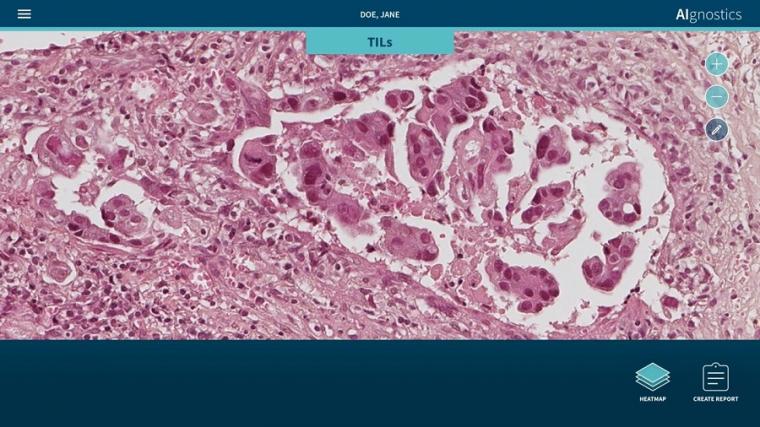
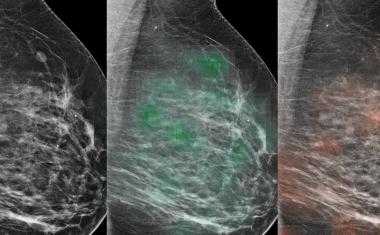
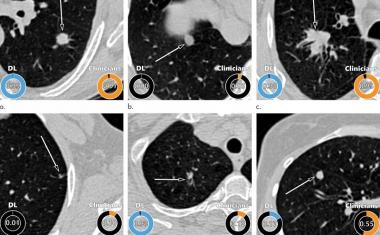
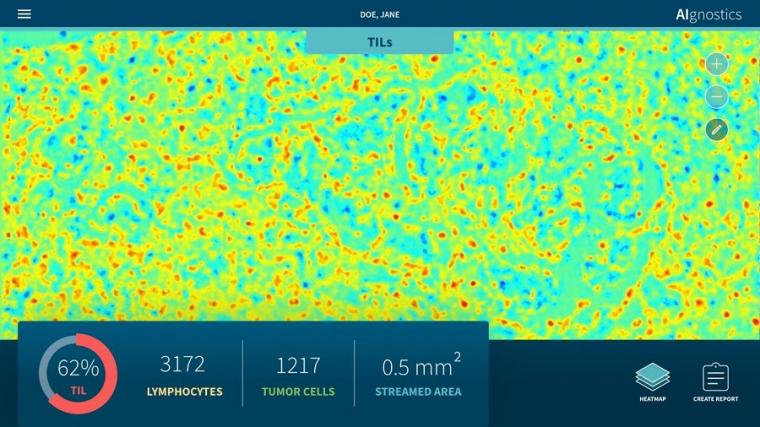
正是这种共生关系使得新发表的方法成为可能。“我们的系统有助于检测显微图像中的病理改变。与此同时,我们能够提供精确的热图可视化,显示微观图像中的哪个像素对诊断算法有贡献,以及在多大程度上有贡献,”Müller教授解释说。该研究团队还成功地进一步开发了这一过程:“我们的分析系统已经使用机器学习过程进行训练,因此它也可以预测各种分子特征,包括DNA的状况,基因表达,以及在组织的特定区域的蛋白质表达,基于组织学图像。
接下来的议程是认证和进一步的临床验证,包括肿瘤常规诊断的测试。然而,Klauschen教授已经确信这项研究的价值:“我们开发的方法将在未来使组织病理肿瘤诊断更精确、更标准化、质量更好成为可能。”
这项研究已经发表在自然机器智能.