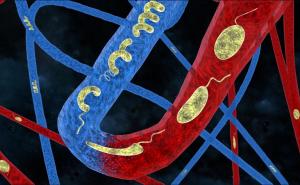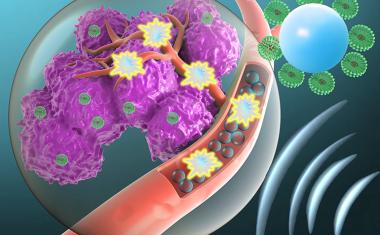
利用同样的现象,科学家们发明了一种微型机扑由于其磁性,它们可以在生理高速血液流动条件下主动向前推进并在血管内导航。“我们的愿景是创建下一代微创靶向药物输送的工具,可以达到更深的组织在体内与更加困难比以前可能访问路线,“说,梅丁·斯蒂物理情报部门主任MPI-IS最后出版的作者。传统的治疗方法遭受非特异性药物在体内分布,他进一步阐述,可能导致严重的副作用在非靶向器官和组织。
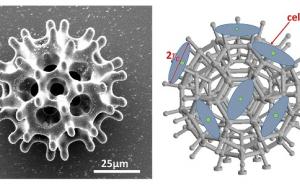
每个微辊的直径小于8微米,由玻璃微粒制成。一边覆盖着一层薄薄的镍和金薄膜,另一边覆盖着抗癌药物分子和可以识别的特定生物分子癌症细胞.“利用磁场,我们的微型机器人可以通过模拟血管上游航行,这是一个挑战,因为强大的血流和密集的细胞环境。目前的微型机器人都不能承受这种流。此外,我们的机器人可以自主识别感兴趣的细胞,如癌细胞。它们之所以能做到这一点,是因为它们的表面覆盖了一层细胞特异性抗体。然后,它们就可以在移动中释放药物分子,”尤努斯·阿拉潘(Yunus Alapan)解释说,他是物理智能部门的博士后研究员,也是该出版物的主要作者之一。
在实验室环境中,微滚轮可以达到每秒600微米的速度——大约每秒76个体长,代表了在这种尺寸下最快的磁性微型机器人。然而,在他们能够在真实场景中执行这个动作之前,有几个挑战需要解决。事实上,它们还远没有在人体中进行测试。在实验室中,该团队能够使用显微镜为机器人成像,并使用电磁线圈引导它们。“然而,目前临床成像模式的分辨率还不足以对人体内部的单个微型机器人进行成像。此外,考虑到微型机器人(约10微米)和目标组织(数千微米)之间的大小差异,单个微型机器人运输的治疗物资是不够的。因此,需要在群体中控制大量微型机器人的操作才能产生足够的效果。但我们离这个目标还很远,”同一系的博士生、这项研究的共同负责人Ugur Bozuyuk说。这仅仅是个开始。
该研究项目的动机可以追溯到诺贝尔奖得主理查德•费曼(Richard Feynman)的著名演讲“底部有足够的空间”。在他的演讲中,这位物理学家设想了一种微米级的机械装置,这种装置可以在血管中穿行,在人体内部进行手术,由此产生了“吞下外科医生”这个词。
在过去的二十年里,由于制造技术、材料使用、驱动和微型机器成像方面的许多飞跃,该研究领域已经加速发展。然而,目前人体内部的微型机器人大多局限于表面组织(如眼睛内部)、相对容易进入的位置(如胃肠道)以及停滞或低速流体环境。尽管条件非常恶劣,但要到达体内更深的地方,可能无法绕过循环系统。科学家们希望他们开发的生物启发策略将有助于为微型机器人在高速血液流动条件下的循环系统中控制导航创造一个新的场所。这可能为微型机器人的靶向和局部治疗铺平道路。