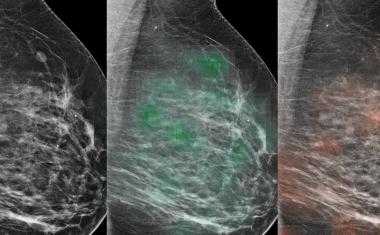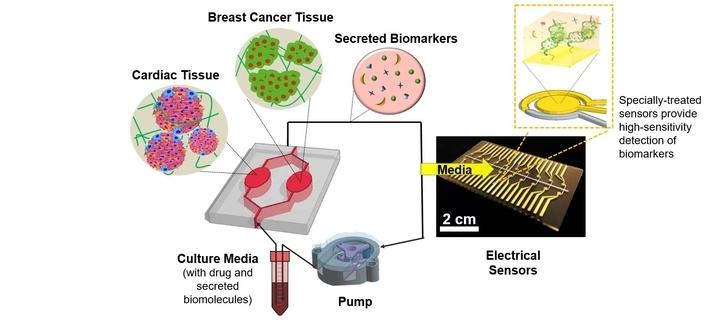
有替代监测可以在实验室模仿身体发生的事情。这些器官的芯片型号包括硅胶芯片,其具有用于培养特异性活的人组织的含量的隔室。隔室连接到微流体通道,氧气和营养介质被泵送和循环。组织细胞通常将称为生物标志物的分子分泌到周围培养基中,这是其健康和功能的良好指标。然后可以测量这些生物标志物的水平以确定组织的状况。
最近,方法已经成功地创建了在选定患者中从乳腺癌药物中监测心脏毒性的简单系统,但迄今为止,迄今为止,有很少的尝试在更大,更全面可靠的模型中生产这样的系统。
一个包括来自Terasaki生物医学创新研究所(Terasaki Institute for Biomedical Innovation)的团队在内的合作团队已经开发出了一种organs-on-a-chip该系统更广泛地检测乳腺癌和心脏组织对治疗乳腺癌药物的反应。在他们的系统中,他们选择了两种由健康心脏细胞产生的心脏生物标记物和一种由活跃生长的乳腺癌细胞产生的心脏生物标记物。这项研究包括对健康和人工诱导的受损心脏组织的测试,以反映乳腺癌患者化疗前可能的心脏状况。他们还为该系统设计了附加功能,以增强其功能。
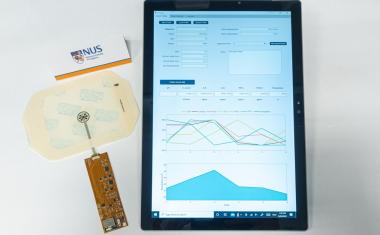
该团队设计了一种芯片系统,分为两个独立的区域,分别用于乳腺癌组织培养和健康或人工诱导的受损心脏组织培养;这些隔室由通道连接,使流体在它们之间自由流动。为了更接近地复制天然机体组织的力学特性,组织培养是通过将心脏或乳腺癌细胞的微小球状体包裹在凝胶状物质中来制备的。芯片循环流体系统的预先控制确保了组织接受氧气、营养介质和化疗药物的输送。
“这项工作建立了监测乳腺癌化疗中心脏毒性的重要模型,”第一作者Junmin Lee,Ph.D.是Terasaki Institute的研究团队的一部分。“我们成功地创建了紧密模仿身体组织的心脏和乳腺癌组织,我们开发了一种改进的传感装置和药物递送系统;这些是芯片技术的里程碑。“
与心脏病或乳腺癌组织的单隔室模型相比,发现与心脏组织的通信中的积极生长乳腺癌组织比在单片机系统中发现的乳腺癌组织减少了健康心脏生物标志物的水平。此外,双芯片系统提供了证据表明乳腺癌细胞的生物标志物分泌不仅受药物治疗而影响,而且通过它们与具有不同损伤水平的心脏组织的相互作用。这表明心脏和乳腺癌组织之间的相互作用对细胞功能和疾病进展的指标具有重要影响。
虽然还不能就暴露于乳腺癌药物后,受损前的心脏组织是否更容易受到心脏损伤得出明确的结论,但结果表明,在健康的心脏组织中,与不使用药物相比,使用乳腺癌药物会导致细胞生长和健康心脏生物标志物的分泌减少。
进一步的试验可以用来探索使用该模型来检测和预测化疗药物的心脏毒性。该模型可以扩展到包括长期培养的组织观察、额外生物标记的检查、使用来自几个患者的组织测试该模型,以及测量心脏损伤的其他非生物标记指标(例如,电和收缩功能)。未来的可能性可能是将肝脏组织组件添加到芯片上,并考虑到系统的可伸缩性,使其与身体系统相关联。
“这些努力为未来疾病模型的应用奠定了重要的基础,”Terasaki研究所主任兼首席执行官Ali Khademhosseini博士说。“我们研究所的个性化生理平台是我们将个性化医疗带到现实世界的众多载体之一。”
来源:寺崎研究所