CRISPR/Cas9技术是基于一种针对噬菌体的细菌防御系统的改良版本。这项技术的一个里程碑式的发现实际上是在维也纳发现的,并于2012年发表在一项由Emmanuelle Charpentier和VBC博士生Krzysztof Chylinski共同撰写的研究中。由于CRISPR/Cas9还具有编辑哺乳动物基因组的能力,它已迅速成为世界各地实验室中使用最多的基因编辑方法,在临床治疗罕见疾病方面具有巨大潜力。就在一周前,镰状细胞性贫血的治疗首次取得成功。
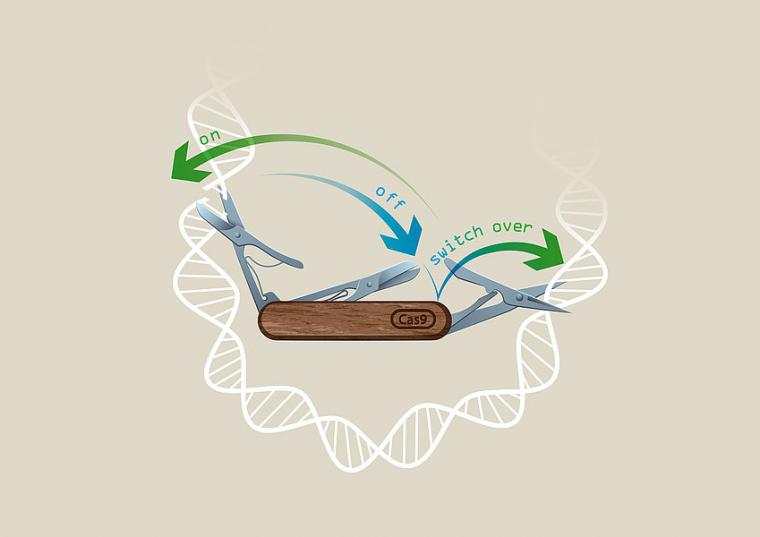
为了控制基因组编辑的能力,几个小组已经在研究控制编辑活动的系统。来自IMBA乌尔里希·埃林(Ulrich Elling)实验室的科学家们现在能够在一个名为“CRISPR-Switch”的系统中,对sgRNA的活动进行前所未有的控制。
CRISPR-Switch系统极大地放大了基于crispr的基因编辑的应用潜力,因为它可以快速启动,而不会出现任何可检测到的泄漏。它还可以规避体内可能的免疫应答,因为它不像以前的方法那样基于Cas9表达的调节。
在来自Elling实验室的CRISPR-Switch中,使用基于Cre-Lox和Flp-FRT重组酶的系统,通过调节sgRNA的表达来实现基因编辑。这些是位点特异性重组系统,允许基因表达的精确位置和时间。Cre和Flp在不同类型的细胞中以其高的重组效率和精度而闻名。
通过使用新的CRISPR-Switch方法,科学家能够以更高的特异性靶向基因,并且由于使用重组酶,一个基因可以在一个选定的细胞类型中被精确地敲除。作为额外的控制水平,多基因现在可以以任何想要的顺序被敲除。这使得CRISPR技术具有前所未有的多功能性,因为基因激活的确切时间可以在体内和体外的不同病理中进行研究。与多伦多Lunenfeld-Tanenbaum研究所的IMBA校友Daniel Schramek一起,作者研究了在小鼠模型中导致胶质瘤形成的诱变事件的顺序。CRISPR-Switch方法用途广泛,可应用于不同类型的肿瘤,从而检测诱导肿瘤形成所需的精确基因序列。这项技术具有不可思议的潜力,它不仅可以研究肿瘤起始,而且可以解决非常具有挑战性的肿瘤维持问题。
该研究的共同第一作者Maria Hubmann解释说:“我们在小鼠体内的研究证实,明确的基因敲除顺序对肿瘤的形成是必要的。我们研究了两个特定的基因,NF1和TRP53,它们被认为与胶质母细胞瘤有很强的联系。只有当我们在NF1之前敲除TRP53,而不是反之,小鼠才会患上胶质瘤。”
“CRISPR-Switch允许我们在空间和时间上控制基因编辑,同时确保一个令人难以置信的快速开关和最小的非特异性影响。维也纳生物中心核心设施的第一作者Krzysztof Chylinski解释说:“我对我们方法的未来应用感到兴奋,因为我相信全世界的实验室很快就会发现它的好处。”
CRISPR-Switch技术也可以作为一个合作机会。IMBA正积极寻求在相关应用领域有商业利益的许可合作伙伴,如筛选、突变分析、更安全的基因组编辑、多路复用和/或体细胞基因治疗。