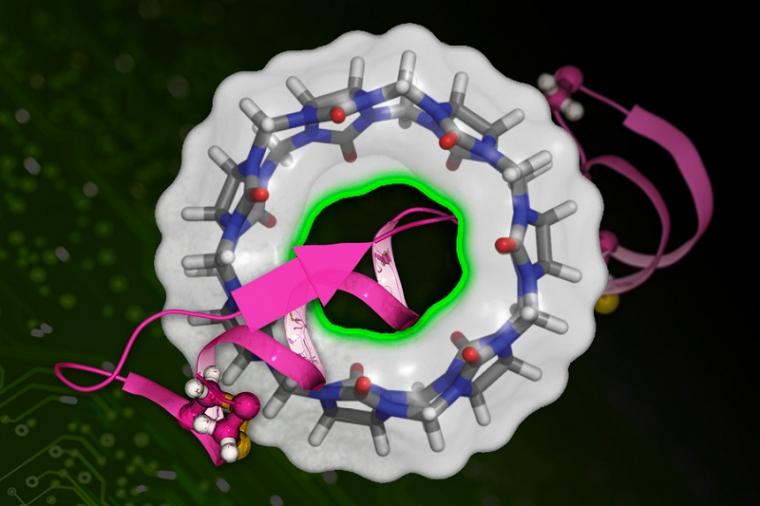
药物只有附着在体内的目标蛋白质上才能起作用。评估这种粘性是药物发现和筛选过程中的一个关键障碍。结合化学和机器学习可以降低这一障碍。
这种被称为DeepBAR的新技术可以快速计算候选药物与其靶标之间的结合亲和性。与之前最先进的方法相比,这种方法可以在很短的时间内实现精确的计算。研究人员表示,DeepBAR有朝一日可能会加快这一进程药物发现和蛋白质工程。
“我们的方法比以前快了几个数量级,这意味着我们可以发现既有效又可靠的药物,”麻省理工学院(MIT)辉瑞-劳巴赫化学职业发展教授、麻省理工学院和哈佛大学布罗德研究所(Broad Institute of MIT)副研究员张斌(Bin Zhang)说。
药物分子和目标蛋白质之间的亲和力是通过一个叫做结合自由能的量来测量的,这个量越小,结合就越粘。“较低的结合自由能意味着药物可以更好地与其他分子竞争,”张说,“这意味着它可以更有效地破坏蛋白质的正常功能。”计算候选药物的结合自由能提供了药物潜在有效性的指标。但这个数量很难确定。
计算束缚自由能的方法分为两大类,每一类都有自己的缺点。一类是精确计算数量,消耗大量时间和计算机资源。第二种方法在计算上不那么昂贵,但它只能得到一个近似的束缚自由能。张和麻省理工学院化学系的博士后丁新强设计了一种方法,使两者兼得。
准确和高效
DeepBAR精确地计算束缚自由能,但它只需要以前方法所需计算的一小部分。这项新技术将传统的化学计算与机器学习的最新进展相结合。
DeepBAR中的“BAR”代表“班尼特接受率”,有几十年的历史算法用于精确计算束缚自由能。使用贝内特接受比通常需要了解两个“端点”状态(例如,与蛋白质结合的药物分子和与蛋白质完全分离的药物分子),以及许多中间状态(例如,不同程度的部分结合),所有这些都降低了计算速度。
DeepBAR通过在被称为深度生成模型的机器学习框架中部署Bennett接受率,大幅削减了那些中间状态。“这些模型为每个端点创建一个参考状态,即绑定状态和未绑定状态,”Zhang说。这两种参考状态非常相似,因此可以直接使用Bennett接受比,而无需所有昂贵的中间步骤。
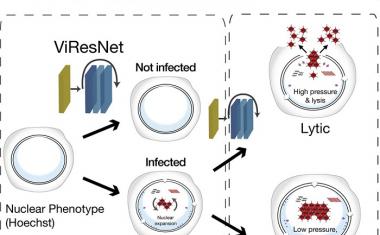
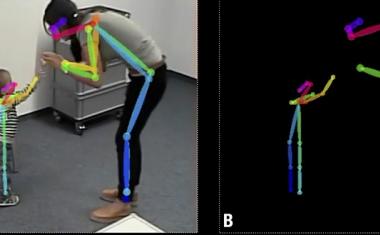
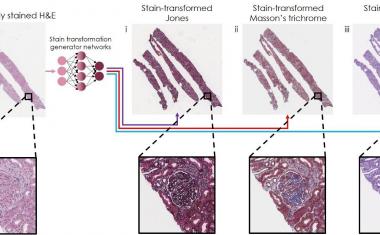
在使用深层生成模型时,研究人员借鉴了计算机视觉.“这基本上与人们用于计算机图像合成的模型相同,”张说。“我们把每个分子结构看作是模型可以学习的图像。所以,这个项目是建立在机器学习社区的努力之上的。”
虽然将计算机视觉方法应用于化学是DeepBAR的关键创新,但这种交叉也带来了一些挑战。“这些模型最初是为2D图像开发的,”丁说。“但在这里,我们有蛋白质和分子——这是一个真正的3D结构。因此,在我们的案例中采用这些方法是我们必须克服的最大技术挑战。”
药物筛选的更快未来
在使用类似蛋白质的小分子进行的测试中,DeepBAR计算的结合自由能比以前的方法快了近50倍。张说,效率意味着“我们真的可以开始考虑使用它来进行药物筛选,特别是在新型冠状病毒肺炎.DeepBAR的精确度与黄金标准完全相同,但要快得多。”研究人员补充说,除了药物筛选,DeepBAR还可以帮助蛋白质设计和工程,因为该方法可以用来模拟多种蛋白质之间的相互作用。
加州大学圣地亚哥分校(University of California at San Diego)的制药科学教授迈克尔·吉尔森(Michael Gilson)没有参与这项研究,他说,DeepBAR是“一项非常好的计算工作”,在将其用于现实世界的药物发现之前,还需要克服一些障碍。他说,DeepBAR需要通过复杂的实验数据进行验证。“这肯定会带来更多挑战,可能需要进一步增加近似。”
在未来,研究人员计划提高DeepBAR计算大蛋白质的能力,这一任务由于计算机科学的最新进展而变得可行。丁磊说:“这项研究是将几十年来发展起来的传统计算化学方法与机器学习的最新发展相结合的一个例子。”“所以,我们实现了以前不可能实现的事情。”
这项研究发表在puböished物理化学快报.
来源:麻省理工学院