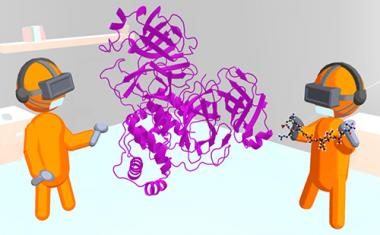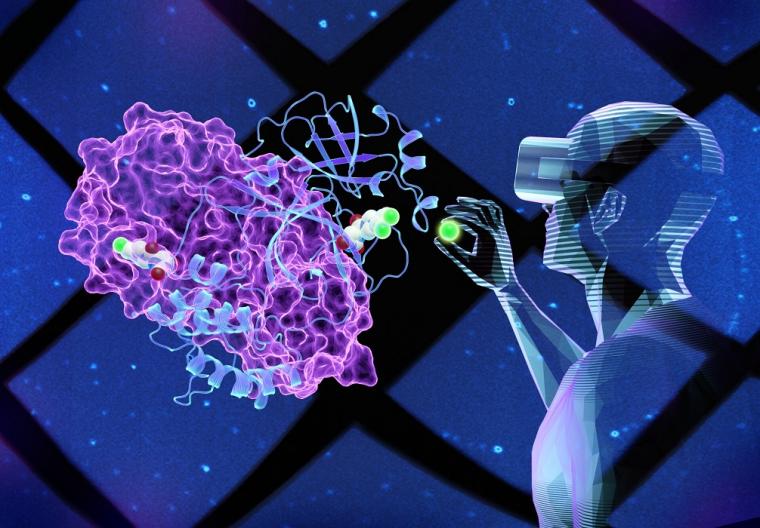
使用虚拟现实为了研究酶的模型,科学家们通过修改它们的结构来构建不同的小分子,看看是否有任何新设计的化合物能够适合或结合到Mpro酶表面的一个关键位点上。足够强的结合可以抑制或阻断这种酶的功能,而这对于阻止病毒在患有艾滋病的患者体内繁殖至关重要新型冠状病毒肺炎.
为了确定特定的化学修饰对19种候选抑制剂与Mpro酶结合紧密程度的影响,研究小组合成了每个抑制剂分子,并测量了它们的结合强度。这种结合越强,抑制剂就越能有效地阻止酶的功能和病毒的复制。
其中一种测试抑制剂,标记为HL-3-68,与其他测试抑制剂相比,证明了具有更好的结合和抑制Mpro功能的能力。
“我们的研究旨在更好地理解分子如何在Mpro酶的活性部位结合,而Mpro酶在SARS-CoV-2复制中发挥着关键作用,”该研究的首席作者丹尼尔·克奈尔(Daniel Kneller)说。“在测试我们设计的分子的过程中,我们发现一种含有一个额外的氯原子,显示出更强的抑制Mpro的能力。这种新的化学结构不同于国际社会以前所研究的结构,它可以为对抗这种疾病开辟新的研究途径,提供令人兴奋的可能性SARS-CoV-2."
Mpro酶上的活性位点对其他类型的冠状病毒来说是常见的,而且似乎不容易突变——这可能为设计针对多种SARS-CoV-2变异和其他变异的抗病毒治疗提供了机会冠状病毒.
同样重要的是,活性部位不同于人类酶中已知的活性部位,这将最大限度地减少可能导致患者产生副作用的非预期结合。
Mpro酶样品的x射线测量和生产由结构和分子生物学中心使用ORNL的散裂中子源(SNS)设施和高通量同位素反应堆(HFIR)的资源进行。候选抑制剂由联合作者Hui Li和Peter Bonnesen在纳米相材料科学中心(CNMS)的高分子纳米材料组合成。
“这项研究结合了大量的生物物理、生化和分子生物学方法,包括虚拟现实辅助结构分析和小分子构建,汇集了来自ORNL、Argonne国家实验室、美国国立卫生研究院和田纳西大学诺克斯维尔分校的科学家。该研究的协作性质允许我们发现小分子抑制剂在与酶结合时必须遵守的规则,以便对药物设计和开发的长期过程中进一步的步骤有用,”通讯作者Andrey Kovalevsky说。
共同通讯作者Peter Bonnesen补充道:“这对CNMS来说是一个新的、令人兴奋的项目,它利用了我们在为用户合成定制有机分子方面的专业知识。对于这个项目,我们一次为我们的SNS同事提供了几个候选分子。由于结果返回分子作为抑制剂的有效性,团队将讨论如何调整分子结构。然后Hui和我会回到实验室,制作这些新的候选抑制剂。”
这项研究还揭示了Mpro酶根据其结合的抑制剂分子的大小和结构,改变其形状和改变其电荷从正电荷到负电荷,或从负电荷到正电荷的能力。这些特征对于开发有效的抑制剂分子非常重要。
在中子散射研究中,科学家们使用了SNS的大分子中子衍射仪(MaNDi),因为它能够从团队必须处理的相对较小的样本中收集数据。
“由于与SARS-CoV-2病毒相关研究的紧迫性,我们只能培养出相对较小的Mpro酶样本,”合著者雷顿·科茨(Leighton Coates)说。由于小样本的中子散射很弱,这导致中子数据“嘈杂”,数据分析可能会很困难。MaNDi仪器的中子束的时间结构使我们能够消除大部分噪声,从而提高信噪比,为我们提供更多有用的数据。”
ORNL研究人员的下一步工作包括测试HL-3-68抑制剂的化学修饰,以确定是否有任何新设计的化合物能够比HL-3-68结合得更好,从而更有效地抑制Mpro酶,并最终阻止冠状病毒的复制。
与此同时,研究人员通过蛋白质数据库公开了他们的数据,以加快向世界科学界和医学界提供信息和帮助。当然,还需要进行更多的研究和测试,以验证任何抑制剂作为COVID-19治疗方法的有效性和安全性。然而,这项研究可以为其他科学家提供一个机会,进行更多的研究,使全世界数十亿人受益。
这项研究发表在药物化学杂志.
来源:橡树岭国家实验室